Update Gentherapie: Geschichte und Ausblick
Liebe Steemianer,
wo stehen wir eigentlich mit der Gentherapie, die ja seit Jahren für viele, teilweise tödliche chronische Krenkheiten eine dauerhafte Heilung verspricht? Ist sie noch Zukunftsmusik oder schon Realität und welchen Patienten kann heute schon damit geholfen werden?

Quelle: https://pixabay.com
Wie genau Gentherapie (1) funktioniert, darauf möchte ich nicht wirklich eingehen, da das ohnehin überall beschrieben steht. Nur soviel: Meist ist die Ursache einer Erbkrankheit der Verlust eines Proteins infolge eines Gendefekts. Statt das Protein regelmäßig (für den Rest des Lebens) zu verabreichen, wie es derzeit gemacht wird (für manche Krankheiten aber gibt es nicht einmal diese Möglichkeit), wird das funktionsfähige Gen mittels Vektoren (in der Regel modifizierte Viren, in die das zu ersetzende Gen eingeschleust wurde) in das Genom des Patienten eingebaut. Dabei können die Vektoren entweder direkt in den Körper injiziiert werden ("in vivo gene editing") oder es werden die Zielzellen (in der Regel Blutzellen) entnommen, mit dem Vektor "infiziert", gereinigt, vermehrt und zurück in den Körper gegeben ("ex vivo gene editing").
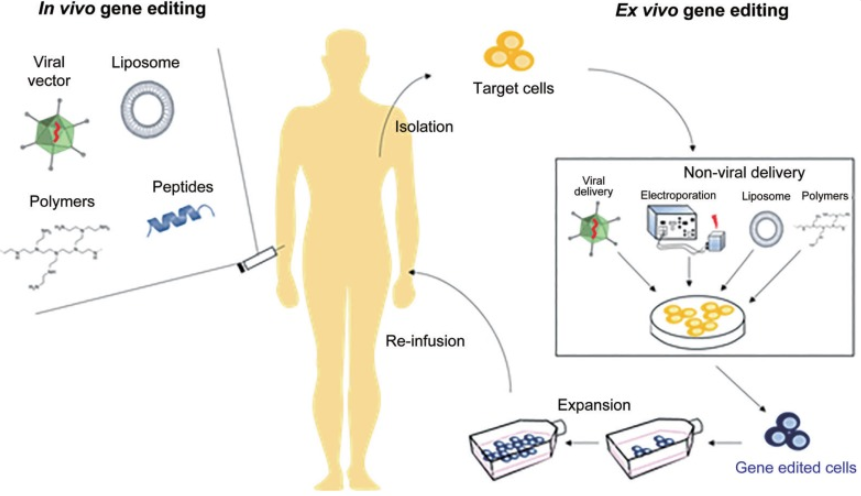
Quelle public domain
Im Idealfall wird das ersetzte Gen dann ausreichend exprimiert, sodass das fehlende Protein auf Dauer zur Verfügung steht. Was im Prinzip einfach klingt, ist aber ungeheuer kompliziert. Z.B. muss man die Patienten mit Viren infizieren, ohne Viruserkrankungen oder gar Krebs zu induzieren. Die Gene müssen so in das Genom eingebaut werden, dass keine Störungen der "benachbarten" Gene auftreten und die target-Proteine in ausreichender Menge exprimiert werden, sie sollen aber keine unerwünschten Immunreaktionen auslösen.
Wenn die Gene in differenzierte Körperzellen oder deren Vorläuferzellen eingeschleust werden, spricht man von Somatischer Gentherapie: Die Therapie bleibt auf den Empfänger beschränkt, die übertragenen Gene können nicht weitervererbt werden. Alle weiter unten beschriebene Gentherapien sind somatische. Das Einbringen von Genen in Keimzellen oder Embryonalzellen eines frühen Entwicklungsstadiums nennt sich Keimbahn-Gentherapie oder Keimbahntherapie, was zur Folge hat, daß die eingebrachten Gene an die Nachfolgegenerationen weitervererbt werden und sich unwiderruflich im Genpool der Menschheit ausbreiten könnten. Die Keimbahn-Gentherapie am Menschen ist in Deutschland und vielen anderen Ländern verboten, wurde aber vor knapp einem Jahr in China angeblich erfolgreich angewendet.
1990: Erste Gentherapie
Die weltweit erste gentherapeutische Behandlung wurde im September 1990 von Ärzten des US-amerikanischen Bundesgesundheitsinstituts an einem vierjährigen Mädchen durchgeführt, nach jahrelangem Genehmigungsverfahren. Die Patientin Ashanti DeSilva litt an einem sehr seltenen schweren kombinierten Immundefekt (engl. severe combined immunodeficiency, SCID), verursacht durch einen Gendefekt sowohl des T- als auch des B-Lymphozytensystems. Diese Kinder haben keine Immunantwort und der kleinste Schnupfen ist für sie tödlich. Sie dürfen nie ihr Plastikzelt verlassen ausser in einem "Raumanzug" (wie im Film "Bubble Boy" geschildert). Die Gentherapie, die aufgrund der begrenzten Lebensdauer der Leukozyten mehrmals im Jahr wiederholt werden muss, ist zwar keine komplette Heilung, ermöglicht den Patienten aber ein Leben ohne strikte Quarantäne. Ohne diese Therapie hätte die erste Patientin nicht überlebt. Sie ist heute 33 und es geht ihr gut.
Rückschläge
1999–2000 wurden erste gentherapeutische Behandlungen in Europa durchgeführt, bei fünf an X-SCID erkrankten Kindern (2). X-SCID ist eine Form der Immunschwächekrankheit SCID, mit ähnlich dramatischem Verlauf, bei der durch eine Mutation das Gen für den Interleukin-Rezeptor-γ-gen defekt ist. Die Gentherapie war zwar erfolgreich, aber zwei der Kinder entwickelten drei Jahre nach der Behandlung eine Form von Leukämie. Da nicht ausgeschlossen werden konnte, dass das reparierte Gen selbst onkogen sein könnte, wird die Gentherapie dieser Erkrankung nur selten durchgeführt.
1999 kam es auch zu einem tödlichen Zwischenfall bei einer von der Uni von Pennsylvania durchgeführten Studie zur Behandlung von Ornithin-Transcarbamylase-Mangel mit Gentherapie. Als Vektor wurden dem 18-jährigen Jesse Gelsinger Adenoviren injiziiert, aber in einer unüblich hohen Dosis von 38 Billionen Partikeln. Es kam zu einer fulminanten Immunreaktion und sein Zustand verschlechterte sich sehr schnell, so dass er nach 4 Tagen an einem Multiorganversagen starb.
Dem leitenden Arzt James M. Wilson wurde von der FDA (US-Arzneimittelbehörde) jede weitere Forschung am Menschen untersagt, auch weil der Patient gar nicht hätte behandelt werden dürfen, da seine Leberwerte die von der Gesundheitsbehörde vorgegebenen Höchstgrenze überschritten hatten (1).
Gendicine - Erste Gentherapie in China zugelassen
Die weltweit erste von einer Behörde zugelassene kommerzielle Gentherapie fand in China in 2004 statt, bei Patienten mit Karzinomen im Kopf- und Nackenbereich und HNO-Tumoren (3). Die von der chinesischen Firma SiBiono GeneTech entwickelte Therapie basiert auf einem Adenovirus als Vektor, in den ein funktionierendes Gen für das Tumorsuppressorprotein p53 eingeschleust wurde. Die Injektionen mit dem Vektor geschehen wöchentlich und i.v. oder direkt in den Tumor.
Laut Hersteller wurden inzwischen tausende Patienten mit Gendicine behandelt und es kam bei mit Gendicine und Strahlentherapie behandelten Patienten dreimal häufiger zu einer kompletten Heilung als bei nur mit Strahlentherapie behandelten Patienten.
Für Kritik sorgten die Umstände, dass der chinesiche Staat Investor bei SiBiono GeneTech war und dessen Leiter bei der Ausarbeitung der Zulassungsrichtlinien für gentherapeutische Medikamente in China beteiligt war. Mittlerweile sind die Zulassungskriterien aber verschärft worden.
Inzwischen forschen viele Firmen an weiteren möglichen Gentherapien mit dem vielversprechenden Protein p53.
Neovasculgen bei Peripherer Arterieller Verschlusskrankheit, made in Russia
2011 wurde diese Gentherapie des russischen Herstellers Human Stem Cells Institute (HSCI) in Russland zugelassen. Die periphere arterielle Verschlusskrankheit (pAVK), engl. peripheral artery disease (PAD) ist eine recht häufige Störung der Durchblutung der Extremitäten durch meist arteriosklerose-bedingter Gefäßverengung ("Verkalkung"). Weltweit sollen 200 Mio. Menschen davon betroffen sein (4).
Bei Neovasculgen wird das Gen, das für den vaskulären endothelialen Wachstumsfaktor (VEGF) kodiert, in einen Plasmidvektor eingebracht. Am Zielort angekommen führt das zu einem Neuwachstum von Kapillaren in sauerstoffunterversorgten (ischämischen) Geweben, zu einer besseren Durchblutung und laut Hersteller konnten dadurch Amputationen eingespart werden. Die Wirkung hält angeblich 3-5 Jahre an und ist gesundheitsökonomisch sogar kostensparend.
Glybera - die erste zugelassene Gentherapie in Europa war ein Mißerfolg
Erst 2012 erhielt die erste Gentherapie die kommerzielle Zulassung in einem westlichen Land: Glybera, für die Behandlung einer seltenen Erbkrankheit, der Lipoprotein-Lipase-Defizienz (LPLD) (5). Europaweit leben kaum mehr als 200 Menschen mit LPLD. Durch das Fehlen der Lipoprotein-Lipase reichern sich Fette im Blut an und können lebensgefährliche Komplikationen auslösen wie etwas heftige Entzündungen der Bauchspeicheldrüse (Pankreatitis). Selbst eine noch so strenge Diät bewahrt die Patienten nicht vor Problemen. Leider wirkt auch die Gentherapie nicht bei allen Patienten, und auch teilweise nur vorübergehend. Da sich aber die Nebenwirkungen in Grenzen hielten und mangels einer wirksamen Alternative wurde Glybera von der EMA (europ. Arnzeimittelbehörde) zugelassen als orphan drug („Arzneimittel für seltene Leiden“) (6). Um einen orphan drug-Status zu bekommen, muß die Indikation so selten sein, dass sich die Entwicklungskosten nicht rechnen würden, dafür wird die Zulassung erleichtert und auch die Patentdauer verlängert.
Eine Behandlung mit Glybera für einen Patienten kostete rund 1 Mio. Euro (abhängig vom Gewicht des Patienten). Da sich nur eine einzige Patientin fand, die mit Glybera behandelt worden war (viele Länder verweigerten angesichts der Kosten und der nicht völlig überzeugenden Wirkung die Erstattung), wurde die Therapie 2017 vom holländischen Hersteller uniQure vom Markt genommen.
Strimvelis - erfolgreiche Gentherapie bei der tödlichen Immunschwäche ADA-SCID
2016 wurde Strimvelis (Hersteller: GSK) zugelassen - eine Gentherapie zur Behandlung von Kindern mit der vererbten Immunschwäche ADA-SCID (7). Der Verlust des Enzyms Adenosin-Desaminase (ADA) blockiert die Entwicklung von weißen Immunzellen und lähmt so die Abwehrkräfte des Immunsystems. Die jährliche Prävalenz in Europa ist nur 15 (15 Kinder werden jeder Jahr mit ADA-SCID in Europa geboren). Die Behandlung ersetzt das fehlende Protein und führt zu einer echten Heilung dieser sehr seltenen, aber absolut tödlichen Krankheit (ohne Behandlung würden die meisten dieser Kinder in den ersten zwei Lebensjahren sterben). In der bisher einzigen Studie mit 18 Kindern sprachen alle 18 an und 14 brauchten auch nach 7 Jahren keine weitere Behandlung mehr.
Vor Strimvelis gab es 2 Optionen: die Transplantation von Knochenmark, doch nicht immer ist ein passender Spender vorhanden und eines von zehn Kindern überlebt diesen Eingriff nicht. Die andere Möglichkeit, die Injektion des fehlenden Enzyms ADA, ist langfristig extrem teuer und auch hier sterben ein bis zwei von zehn Kindern trotz Behandlung.
Trotz des unbestrittenen Nutzens von Strimvelis wurde erst eine Handvoll Kinder damit behandelt. Die Behandlung ist zwar in der gesamten EU zugelassen, darf aber aufgrund des komplizierten Verfahrens nur in einer einzelnen Klinik in Mailand durchgeführt werden. Dieser Engpass erschwert die Anwendung deutlich. Der Preis von 600.000€ erscheint hoch, aber ist wesentlich günstiger als die (lebenslange) Ersatztherapie mit dem ADA-Enzym (jährlich bis zu 400.000€!).
Luxturna - Gentherapie gegen frühkindliche Erblindung
Die Gentherapie Luxturna (Hersteller: Spark) lindert eine Form der Erblindung, Retinitis pigmentosa, die durch einen Defekt im Gen RPE65 verursacht wird (8). Diese seltene Erbkrankheit (in Deutschland gibt es ca. 200 Betroffene), die sich bereits im frühen Kindesalter bemerkbar macht mit Nachtblindheit, führt zum allmählichen Verlust der Sehschärfe und Verengung des Sehfeldes, bis zur vollständigen Erblinden im Alter von etwa 20 Jahren bei den meisten Patienten. Das betroffene Gen kodiert für ein Protein, das für die Funktion des Sehpigments Rhodopsin notwendig ist.
In klinischen Studien wurde Luxturna bislang an 41 Patienten getestet. Bei den meisten Teilnehmern verbesserte sich die Sicht in der Dunkelheit deutlich, aber die Sehschärfe im Hellen leider gar nicht. Zwar hat sich die Lebensqualität der meisten Patienten spürbar verbessert, von einer Heilung kann aber keine Rede sein.
Im März 2018 wurden in den USA die ersten Kinder mit Luxturna behandelt, in Europa finden noch Preisverhandlungen statt (die Kosten in den USA sind 850.000$ pro einmaliger Therapie, es soll aber Rabatte geben bei Nichtansprechen). In allen Ländern ausserhalb der USA übernimmt Novartis den Vertrieb. Der Preis ist insoferne strittig, als neben der nicht vollständigen Heilung es auch noch unklar ist, wie lange die Wirkung anhält.
Luxturna wird mit einer Kanüle unter die Netzhaut der Augen injiziert. Nebenwirkungen gibt es nur lokale, die aber nur vorübergehend sein sollen.
Roche ist derzeit in Verhandlungen, die Firma Spark Therapeutics (die führend bei verschiedenen Gentherapien ist) zu übernehmen, für ca. 4,3 Mrd€.
Kymriah: Gentherapie gegen ALL und Lymphome
Kymriah (Hersteller: Novartis) wurde als weltweit erste CAR-T-Zelltherapie im Jahr 2017 in den USA zugelassen für die Behandlung der akuten lymphatischen Leukämie (ALL), im Mai 2018 dann auch für Non-Hodgkin-Lymphome mit Beteiligung von B-Zellen (B-Zell-Lymphome) . In Europa erfolgte die Zulassung im August 2018 (9).
ALL ist eine eher seltene Form von Blutkrebs (Inzidenz in Deutschland ca. 1000 pro Jahr), bei der sich die B-Lymphozyten des Immunsystems unkontrolliert vermehren. Die Aussichten für das Überleben sind mittlerweile recht gut, etwa 9 von 10 ALL-Patienten können geheilt werden. Bei besonders aggressiven Formen sind die Erfolgsraten allerdings wesentlich geringer. Kymriah ist für diese schweren Fälle gedacht: In einer Studie wurden 79 Patienten unter 25 Jahren damit behandelt, und bei 82% waren nach drei Monaten alle Anzeichen von Krebs verschwunden. Bei der Behandlung von B-Zell-Lymphomen in erwachsenen Patienten war der Nutzen nicht ganz so hoch, aber immer noch wesentlich besser im Vergleich zu Standardtherapien. Eine Studie mit knapp 100 Teilnehmern zeigte nach 19 Monaten, dass vier von zehn Patienten frei von Krebszellen waren.
Bei der Therapie werden körpereigene T-Zellen (Immunzellen, die für den Kampf gegen Krebs wichtig sind) dem Körper des Patienten entnommen und im Labor mit einem künstlichen Rezeptor ausgestattet, dem chimeric antigen receptor (CAR). Dieser trägt bei Kymriah einen Rezeptor für das Molekül CD19, das auf den Krebszellen der ALL-Patienten zu finden ist. Die so gewappneten CAR-T-Zellen werden für wenige Wochen im Labor vermehrt und dann den Patienten zurückgegeben. Mit Hilfe dieses künstlichen Rezeptors können die CAR-T-Zellen alle CD19-tragenden Zellen im Körper identifizieren und beseitigen. Leider tragen auch B-Lymphozyten dieses Molekül, sodass diese Zellen auch beseitigt werden und als Nebenwirkung ein Immundefekt entsteht, der aber durch die regelmäßige Transfusion von Antikörper-Präparaten ausgeglichen werden kann. Es kann auch bei bis zu der Hälfte aller Patienten ein sog. Zytokinsturm - eine schwere bis lebensbedrohliche systemische Entzündungsreaktion, auftreten.
Da diese Therapie (bei B-Zell-Lymphomen) eine Konkurrenz zu Yescarta ist, kostet sie in den USA deutlich weniger als die von ALL, wo es keinen Mitbewerber gibt (in den USA kostet die ALL Therapie mit Kymriah 475.000$, die von Non-Hodgkin-Lymphomen "nur" 373.000$). Die Preisverhandlungen in Europa sind noch nicht abgeschlossen.
Yescarta: CAR-T-Zellen bekämpfen B-Zell-Lymphome
Die Gentherapie Yescarta (Hersteller: Kite/Gilead) nutzt ebenfalls CAR-T-Zellen, um B-Zell-Lymphome zu bekämpfen. In Deutschland erkranken ca. 16000 Menschen jährlich an diesen malignen Lymphomen, das mittlere Erkrankungsalter liegt bei etwa 70 Jahren (10). Die Behandlung erfolgt meist durch eine Strahlen- oder Chemotherapie, über 60% der Betroffenen überleben länger als fünf Jahre. Bei einem Rückfall verschlechtern sich die Heilungschancen jedoch rapide, und nur für diese Fälle ist Yescarta zugelassen, das das gleiche target-Molekül CD19 wie bei Kymriah verwendet. Bei einer Studie mit etwas über 100 Teilnehmern reagierten etwa 8 von 10 Patienten zumindest teilweise auf die Therapie, bei etwa 60% der Patienten wurde das Lymphom vollständig zurückgedrängt. Die mittlere Lebenserwartung betrug etwa zwei Jahre - bei einer historischen Vergleichsgruppe waren es nur sechs Monate.
Die Nebenwirkungen sind bei Yescarta neben den Zytokinstürmen auch Anämie und ernsthafte neurologischen Probleme.
Das Produkt ist seit August 2018 in Europa zugelassen, aber noch kein Preis festgelegt (Stand Juni 2019).
In den USA kostet die Therapie 373.000$ (preisgleich mit Kymriah).
Zolgensma - Das teuerste Medikament der Welt
Im Mai 2019 erhielt Novartis von der FDA die Zulassung für Zolgensma, einer Gentherapie gegen spinale Muskelatrophie (SMA) (11).
Ursache dieser Erkrankung ist ein Defekt in dem Gen SMN1. Erbt ein Kind defekte Genkopien von beiden Elternteilen, können Motoneuronen - spezialisierte Nervenzellen im Rückenmark - nur kurz überleben. Ohne diese Motoneuronen können sich die Muskeln nicht richtig entwickeln. Bei der schwersten Verlaufsform, dem Typ I, sterben die Kinder meist innerhalb der ersten zwei Lebensjahre an Atemschwäche.
Seit 2017 gibt es ein Medikament der Firma Biogen - Spinraza, das den Muskelschwund deutlich vermindert. Es wird alle vier Monate in die Rückenmarksflüssigkeit injiziert, die Jahrestherapiekosten sind bis zu 500.000€.
Bei Zolgensma wird das funktionierende Gen SMN1 in Körperzellen mittels adenoviralen Vektor eingeschleust.
Zolgensma wird einmalig i.v. appliziert und gelangt über das Blut in das Rückenmark, wo die Adenoviren die kranken Motoneuronen "infizieren".
Die bisherige Daten deuten an, dass die Wirkung von Zolgensma und Spinraza vergleichbar gut ist, bei relativ wenigen Nebenwirkungen. Möglich wäre auch eine Kombination der beiden Therapien (falls das finanziell leistbar ist).
Datenmanipulationen - peinlich für Novartis
Entwickelt wurde Zolgensma von der US-Firma AveXis, 2018 übernahm Novartis die Firma für 8,7 Mrd$.
Nun stellte sich heraus, dass Novartis schon vor Erhalt der Zulassung, im Oktober 2018 darauf aufmerksam geworden war, dass es bei Mausversuchen für Zolgensma zu "Unstimmigkeiten mit Daten" gekommen war. Offenbar waren Daten aus bestimmten Tierversuchen manipuliert worden (es handelte sich um 50 Labormäuse). Novartis hatte den Herstellungsprozess von Zolgensma verändert, und diese Versuche sollten die Äquivalenz beider Verfahren validieren. Die FDA reagierte sauer und verlautbarte, sie werde "ihre volle Autorität einsetzen und falls nötig auch zivil- oder strafrechtlich aktiv werden" (12). Da aber die Manipulation kein Auswirkungen auf die Sicherheit und die Wirksamkeit des Medikaments hatten (die Daten waren zur Zulassung auch nicht benötigt worden), sah die FDA von einem Verbot von Zolgensma ab. Insgesamt ein Dämpfer für das Image von Novartis - noch dazu beim teuersten Medikament der Welt. Die Datenmanipulation ist auch ein Wahlkampfgeschenk für die demokratische Präsidentschaftskandidatin Elizabeth Warren, die schon lange gegen zu hohe Medikamentenpreise wettert.
In den USA kostet Zolgensma 2,125 Mio$, zahlbar in fünf jährlichen Raten - noch nie war eine einmalige Verabreichung eines Medikaments teurer! Zu den Kosten hier die interessante Analyse eines betroffenen SMA-Patienten.
Zynteglo - in Rekordzeit zugelassene Gentherapie gegen β-Thalassämie
Aufgrund des großen Bedarfs an wirksamen Therapien (Inzidenz der Erkrankung in Europa 1:10000) wurde das Orphan Drug Zynteglo des Herstellers Bluebird Bio in nur 150 Tagen von der EMA beurteilt und im März 2019 bedingt zugelassen (endgültige Zulassung erfolgt, wenn mehr Daten vorliegen) (13).
Bei dieser Therapie werden dem Körper hämatopoetische Stammzellen entnommen und mit einem lentiviralen Vektor ein modifiziertes β-Globin-Gen eingeschleust. Den Patienten fehlt nämlich dieses Gen, ohne das kein β-Globin gebildet werden kann. Das Fehlen dieses Hauptbestandteils von Hämoglobin führt bei diesen Patienten zu chronischer Anämie. Die Alternative, lebenslange regelmäßige Bluttransfusionen schädigen den Körper auf Dauer. Der einzige kurative Ansatz ist eine hämatopoetische Stammzelltransplantation, für die sich aber nicht immer ein passender Spender findet.
In zwei Studien hat sich Zynteglo bei 80% der Patienten als wirksam erwiesen (die Notwendigkeit von Bluttransfusionen gesenkt), die Nebenwirkungen waren vertretbar. Für Patienten ab 12 Jahren mit einem anderen als dem besonders schwer verlaufenden Genotyp β0/β0 erhielt Zynteglo die bedingte Zulassung. Der Preis: max. 1,575 Mio€, zahlbar in fünf jährlichen Raten - sollte die Wirkung von Zynteglo weniger als fünf Jahre anhalten, werden alle noch ausstehenden Zahlungen erlassen (14). Erste Patienten sollen ab 2020 behandelt werden.
Kosten
An den angegebenen Kosten sieht man, was für eine Herausforderung die neuen Therapien für die Zahler und Krankenkassen bedeuten. Unsere Gesundheits- und Kostenerstattungssysteme wurden geschaffen für regelmässige geringe Kosten, für simple Medikamente, die über einen langen Zeitraum eingenommen werden, nicht für riesige Einmalzahlungen. Die meisten würden aber einer Therapie, die nur einmal verabreicht werden muss, vorziehen vor einer lebenslangen (die oft nicht kausal ist und nur lindert statt heilt). Deshalb ist die Erwartung, dass der langfristige Nutzen dieser einmaligen Therapien die hohen Kosten rechtfertigen sollte, insbesondere beim Einsatz flexibler Modelle wie Ratenzahlungen und Rabatte bei Nichtansprechen bzw. „Pay-for-Performance“.
Alle bisher zugelassenen Gentherapien waren bei relativ seltenen Indikationen. Spannend wird es aber, wenn eine Gentherapie erfolgversprechend ist, die eine wesentlich größere Zielgruppe hat. Bei vielen Arten von Krebs ist das der Fall. Da diese potentiellen "Blockbuster" für die Pharmafirmen lukrativ sind, wird sich dort mehr Konkurrenz finden, was zu einer natürlichen Gegenregulation beim Preis führen könnte (wie man bereits bei Kymriah / Yescarta gesehen hat).
Ausblick
Derzeit werden weltweit zahllose klinischen Studien mit rund 300 gentherapeutischen Kandidaten durchgeführt. https://clinicaltrials.gov listet 751 Studien auf, die Mehrheit davon erst in Phase 1, also noch Jahre von einer Zulassung entfernt. Adenoviren und Retroviren sind die am häufigst benutzen Vektoren. Das Ziel der meisten Studien ist die Behandlung von Krebs.
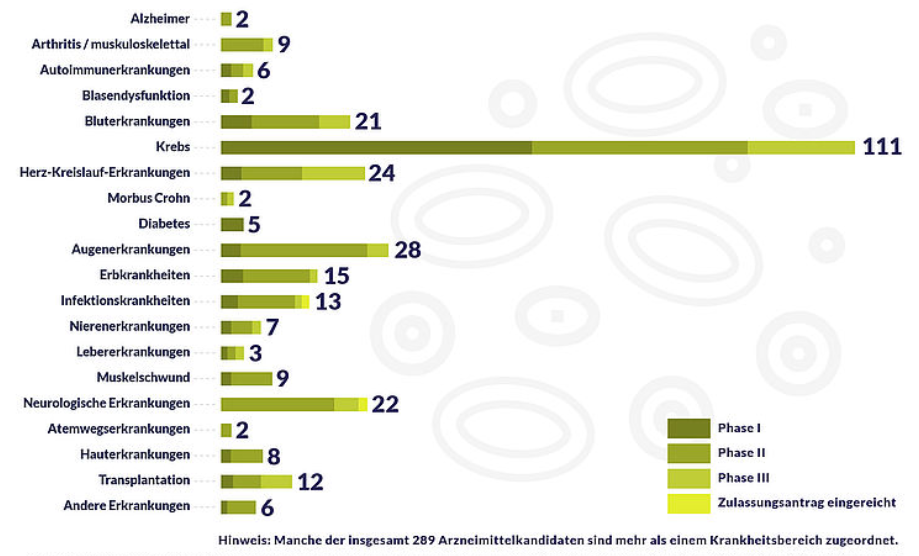
Übersicht über die Indikationsgebiete der rund 300 gen- und zelltherapeutischen Programme Quelle Stand: Jan 2019, nicht kommerzieller Gebrauch gestattet
Z.B. soll schon nächstes Jahr eine langerwartete Gentherapie für Hämophilie auf den Markt kommen (Prävalenz von Hämophilie A (diesen Patienten fehlt Faktor VIII) bei Männern ca. 1:5000, von Hämophilie B (hier fehlt Faktor IX) ca. 1:30.000). Eine von Spark/Pfizer gesponserte und im New England Medical Journal publizierte Studie bei Hämophilie B hatte schon 2017 gute Ergebnisse geliefert: Nach rund einem Jahr benötigten 8 der 10 behandelten Patienten keinen Ersatz-Faktor IX mehr und 9 hatten keine einzige Blutung (davor hatten sie ca. 11 Blutungen pro Jahr, trotz regelmäßiger Faktor IX-Gabe!). Einzige Nebenwirkungen waren ein Anstieg mancher Leberwerte, der eine Prednisolontherapie erforderlich machte (15). Mindestens drei weitere Pharmafirmen forschen derzeit intensiv an dieser Indikation. Es wird interessant sein zu beobachten, wie sich das auf den Preis dieser Therapien auswirken wird.
Einige Projekte verwenden auch die schon berühmt gewordene "Genschere" Crispr-Cas9. So wurde im Oct. 2018 in Science publiziert, dass an einem Hundemodell der Erbkrankheit Duchenne-Muskeldystrophie mittels Crispr-Cas9 das defekte Gen, das für Dystrophin kodiert, erfolgreich repariert werden konnte. 8 Wochen nach einer Einmalanwendung war 80% der Dystophin-Expression wiederhergestellt, Werte über 15% führen schon zur wesentlichen Verbesserung der Symtome (16). In diesem Fall wurde also kein neues Gen eingesetzt, das das defekte ersetzen sollte, sondern das defekte Gen durch gezielte Nukleotidveränderungen an der DNA in vivo repariert. Noch ist es aber zu früh, um gene editing mit Crispr-Cas9 breit am Menschen anzuwenden, da nicht ausgeschlossen werden kann, dass auch an anderen Stellen in der DNA unbeabsichtigte Veränderungen stattfinden, und dass diese vermutlich dann irreversibel wären. In diesem Zusammenhang hat kürzlich die Alliance for Regenerative Medicine’s (ARM) Gene Editing Task Force neue Richtlinien zum gene editing herausgegeben, in denen zwar somatisches gene editing unter bestimmten Bedingungen befürwortet, aber unter anderem nochmals betont wurde, dass Keimbahntherapien derzeit nicht vertretbar sind (17).
Man sollte übrigens nicht vergessen, dass fast alle derzeitigen Ansätze als Ziel monogenetische Erkrankungen haben, also solche, die auf einem einzigen fehlerhaften Gen basieren. Erkrankungen, die durch komplexere genetische Schäden ausgelöst werden, wie zum Beispiel Trisomien oder viele Krebsarten, können mit den derzeitig entwickelten Gentherapie noch nicht ursächlich behandelt werden. Ganz zu schweigen von Erkrankungen, deren Ursache wir gar nicht kennen, wie z.B. Arterielle Hypertonie vulgo Bluthochdruck.
Dennoch, aufgrund der Fülle an Projekten ergibt sich, dass die Medizin von morgen einer Revolution gegenübersteht, die aufgrund der bisherigen vereinzelten Erfolge der Gentherapie nur erahnt werden kann. Besonders die wirksame Bekämpfung von etlichen Krebsformen - DIE Herausforderung in der Medizin schlechthin - wird zwar nicht einfach und noch einige Zeit dauern, aber wird letztlich für hunderte Millionen Menschen lebensverlängernd sein. Man denke nur an Lungenkrebs, der für jeden 4. Krebstoten weltweit verantwortlich ist. Auch hier gibt es schon erste gentherapeutische Ansätze (18).
Das heißt aber, dass nicht nur die gewaltigen Therapiekosten zu bewältigen sind, sondern die Gesundheitskosten insgesamt werden durch die höhere Lebenserwartung explodieren (je älter, desto multimorbider werden Menschen). Kein Politiker hat sich meines Wissens darüber bereits Gedanken gemacht. Absurderweise werden jedes Jahr Budgets fürs jeweils nächste gemacht, ohne einen langfristigen Plan zu haben. Ob das gut geht?
Quellen:
(1) https://de.wikipedia.org/wiki/Gentherapie
(2) https://de.wikipedia.org/wiki/X-SCID
(3) https://de.wikipedia.org/wiki/Gendicine
(4) http://eng.hsci.ru/products/Neovasculgen
(5) https://www.wissensschau.de/genom/gentherapie_glybera_lipoproteinlipase-defizienz.php
(6) Als selten gilt in Europa 5 Fälle pro 10000 Einwohner https://de.wikipedia.org/wiki/Orphan-Arzneimittel
(7) https://www.wissensschau.de/genom/gentherapie_strimvelis_ada-scid.php
(8) https://www.deutsche-apotheker-zeitung.de/news/artikel/2018/11/23/gentherapie-gegen-erblich-bedingte-augenerkrankung-in-der-eu-zugelassen
(9) https://www.wissensschau.de/krebs_tumor/car-t-zellen_kymriah_leukaemie.php
(10) https://www.wissensschau.de/krebs_tumor/car-t-zellen_yescarta_b-zell-lymphom.php
(11) https://www.wissensschau.de/genom/gentherapie_zolgensma_spinale_muskelatrophie.php
(12) https://www.bilanz.ch/unternehmen/novartis-im-us-wahlkampf-werden-aus-labormausen-elefanten
(13) https://www.pharmazeutische-zeitung.de/gruenes-licht-fuer-gentherapie/
(14) https://www.fiercepharma.com/pharma/bluebird-prices-gene-therapy-zynteglo-at-eu1-575m-europe-to-be-paid-over-5-years
(15) https://www.nejm.org/doi/10.1056/NEJMoa1708538
(16) https://science.sciencemag.org/content/362/6410/86?rss=1
(17) http://www.genetherapynet.com/gene-therapy-news/637-gene-therapy-developers-issue-principles-for-human-genome-editing.html
(18) http://www.genetherapynet.com/gene-therapy-news/635-gene-therapy-making-waves-for-lung-cancer-patients.html
Wer bei aktuellen Entwicklungen in der Genherapie auf dem Laufenden sein will, schaut ab und zu hier rein:
http://www.genetherapynet.com/
Source
Copying/Pasting full or partial texts without adding anything original is frowned upon by the community. Repeated copy/paste posts could be considered spam. Spam is discouraged by the community, and may result in action from the cheetah bot.
More information and tips on sharing content.
If you believe this comment is in error, please contact us in #disputes on Discord
Where in the text did I do this "Copying/Pasting full or partial texts without adding anything original".
I spent hours on this article going over many sources, cited them all and selected the essentials in order to present this topic in a readable way and presented an outlook (is the outlook also not original?). Naturally I had to paste some items, how else e.g. I can describe a disease, by creating different symptoms than the existing ones? You won´t find in German language a single article that covers all this. To name this plagiarism is ridiculous. Please reconsider or I will leave.
@twinner @balte das kann es echt nicht sein, dass ich in einen Topf mit Spammern geworfen werde.
Wenn das so ist, pfeiffe ich drauf und das wars mit Steem für mich.
Hi,
You post has been reported by the community. It is not the first time you were reported for this.
deutsch/@stayoutoftherz/newsflash-erdogan-beleidigt-araber-clans-in-problemvierteln-oekostudie-zum-hambacher-forst-ufo-enttaeuschung
Majority of text in this article is copypasta from the sources. Personal thought makes only about 5-10% of your articles.
Also, you just dumped sources in the end or randomly put them in the text without exactly specifying each part of the text is sourced.
This is not the way articles are written, especially academic ones.
Many parts of your articles can be considered as plagiarism as neither the text is clearly put in apostrophes to specify it is quote, nor the exact source next to quote text is given.
Just an example from this article.
The text is evidently re-written or spun from Wikipedia article:

Although you gave the source to Wikipedia article in the end, the text is not your own writing from your head, but simple re-writing of text from the source changing the structure of sentences and word placements. You have not put your text in quote marks highlighting it and didn't give number reference to the highlighted text.
Your articles are full of these text manipulations making it look like it is all your thought while it is not nothing more but re-written text.
If you tried to write something like that at any university as academic or student, it would be right away rejected, and you would possible face disciplinary consequences.
If you continue to write such deceitful articles for curated tags such as stem, steemstem (they clearly stated that your articles do not comply with rules), science, etc; we will have to downvote it if reported again by the community.
Please improve the writing.
Dear logic,
his article is not written for an scientific journal, he gives the source and your example seems wrong to me, there are new aspects in it, i do not read anything about the bubble boy in wikipedia, for example.
Thats how you will loose more and more steemians,.
He started a power down now-respect!
He is also a good curator for the german speaking community and he wrote about a lot of different interesting topics, but you hunt him, respect! .
Our own content -by the way-are mainly actifit-reports with one photo, respect!
And 0,40 rewards for the auto-reply from steemcleaners are okay, of course, respect!
Go on like that, respect!
Best regards!
Mann die habens aber jetzt richtig abgesehen nun auch noch der unlogische logic !
Wie gesagt wtf!
der v.a actifit reports mit einen photo postet-super!
Kommt noch Heute ein Post von steemit-total über den Fall darüber!
Bitte um Unterstützung!
Volle!!! Unterstützung.
No one is hunting anyone here. He got reported by the community so the community does not agree with the way he writes.
No one is asking him to write for scientific journal. He is writing for science projects on Steemit that have specific rules. He has chosen to to so by selecting curated tags in this category.
He was only asked to improve writing or alternatively he can choose to keep doing the same, but then he should not apply for curation from specific projects if he cannot follow their rules.
It's immature to start powering down jut because he got downvoted on one past. Maybe he is just incapable of improving the content.
I will remove the flag as favour but if he gets reported again, we will have to act.
Thanks for removing the flag. Be ensured that I will not use the stem, steem-stem, de-stem and science tags anymore and that I won´t curate scientific content anymore.

But be also ensured, that if I decide to stay (I have to sleep over it) I will check such content, and if I find a verbiage that is not referenced and highlighted "exactly specifying each part of the text", then I will flag and give you a mention in a comment.
A recent example. This article on steemstem.io did quote a source without referencing it. Is this OK for you?
It is sad, as I wrote many scientific articles in the past and never had any problems. My approach is a more journalistic one, to try to bring science content to non-scientists, but if this is not appreciated then so be it.
Hi, thanks a lot for you reply.
I will check that article up now. Thanks for reporting.
Feel free to report abuse on our website (providing sources). Better not to just tag us as we are likely not to notice mention under the post.
It's the best to report it here.
http://steemcleaners.com/reports/new
I cannot find any source of plagiarism. Would you please give me source from which it is plagiarised.
Steemit article appear to original and belonging to the person owning the blog wissensagentur.net.
Everything quoted seems to be properly put in quote markdown and sourced right next to marked text.
The personal thought parts does not seem to be found anywhere else. It may be plagiarism but I cannot find it yet. Your source would help
Danke für den informativen Artikel-für den steemcleanersdownvote sehe ich wirklich keinen Grund-natürlich bist du weder ein Spammer und ein c&p autor-weis jeder der Deine Artikel hier schon lange liest, das Agieren der "steemcleaners" ist hier ungerecht und kontraproduktiv
Ich habe leider oder zum Glück keinen Draht zu denen-kann den Artikel upvoten (hätt ich sowieso + re-steemen (das sollte diskutiert werden) + boostern (da kommen ev. dann noch ein paar kleinere downvotes wegen tipu-gegnern), mal sehen, aktuell haben sie ihn dir ja auf null runtergecleant, so verscheucht man zielgerichtet User.
BGvB!
und was noch auffällt 0.43 cent für den steemcleaners auto-comment, 0,40 Cent bekommen die auf jeden auto-kommentar, naja, was soll man dazu sagen!! BGvB!
Das ist mal wieder richtig Scheiße (sorry) da fällt mir kein anderes Wort ein!
aber @stayoutoftherz hat doch alles richtig gemacht!
Er hat alle Quellen die Zitiert wurden angegeben!
Du und @twinner hat ja schon gegen gevotet und immer noch unsichtbar!
Wenn wir nun nen Bot draufsetzen bringt es auch nichts weil dann die downvotes kommen!
wtf ist das die Zukunft von Steenit?!
Gebe Dir vollkommen Recht! Da unterstütze ich auch sehr gerne mit 100%.... 💪
Ich hab logic auch ein paar Zeil dazu geschrieben, siehe unten.
Unmöglich finde ich das!
So macht man die Freude hier eben kaputt.
BGvB!
Kaum ist man ein paar Stunden weg, geht hier die Post ab. Vielen Dank an Dich und @miketr für die Unterstützung.
!BEER
View or trade
BEERat steem-engine.Hey @stayoutoftherz, here is a bit
BEERfor you. Enjoy it!Sorry, hab das erst zu spät gesehen, aufboostern mit tipu geht nicht mehr, zu alt der post. Auf den Discord mit denen zu diskutieren bringt nix, kann nur noch den Kommentar upvoten, re-steem hab ich gemacht.
Dass wäre wirklich ein interessanter Post gewesen, wäre hier nicht von hier und da kopiert geworden. Wirklich schade, da es sich um ein sehr spannendes Thema handelt!
Alleine die Abschnitte
bestehen zu einem guten Viertel aus Copy/Paste mit zum Teil etwas verdrehten Wörtern um eine Originalität zu suggerieren. Mehr habe ich mir bis jetzt gespart, da der Post damit schon in einem Bereich liegt, der meiner Meinung nach nicht mehr OK ist. Das Übernehmen von Text ist OK, wenn die Quelle es gestattet, aber dann bitte deutlich als Zitat kennzeichnen und nicht als eigenen text verkaufen.
Bitte verwende auch nur Bilder, die für die kommerzielle Verwendung frei sind. Dadurch, dass du eine Leistung für deine Posts erhälst, bist du mehr oder weniger kommerziell tätig. Richtig sicher ist es deshalb nur entsprechendes Bildmaterial zu verwenden.
Solltest du denken, dass es sich um einen Fehler handelt, dann können wir das gerne hier in den Kommentaren oder im Discord ausdiskutieren.
Gerne kannst du dich nach der Überarbeitung des Posts bei mir melden, dann schaue ich es mir nochmals an.
Du erinnerst dich bestimmt daran, dass das nicht dein erster Post ist, der im Grunde auf kopierten Textbausteinen basiert. Ich rate dir weiterhin dringendst, dich mit einem @steemstem Mentor zu beraten. @chappertron oder @sco können dir aber bestimmt auch beratend zu Seite stehen oder dir einen deutschsprachigen Mentor empfehlen.
Es ist mir herzlich egal, welche Meinung Du zu dem post hast. Ich wollte einen kurzen, aber vollständigen Abriss zur Entwicklung der Gentherapie geben und klar habe ich einzelne Sätze verwendet aus den angegebenen Quellen. Du hörst Dich an wie ein Mathelehrer, der seine Schüler zwingen will, alles mit der Hand zu rechnen, statt für primitive Dinge einen Taschenrechner zu verwenden. Das meiste habe ich ohnehin zusammengefasst und umformuliert. C&p sieht anders aus, da hätte ich nicht Stunden an dem Artikel sitzen müssen. Weil Du Neovasculgen erwähnst, da gibt es im deutschen Sprachraum (warum eigentlich) ja so gut wie gar nichts, wo soll da ein c&p herkommen?
Unter 5$ für so einen post ist Deiner Meinung nach nicht in Ordnung und ein Käferfoto mit 2$ schon? Das ist ja ein Witz.
Und zur Lizenz: Das ist für mich kein kommerzieller Bereich, für Dich vielleicht schon, Dein Pech.
Ich denke gar nicht daran, den post zu überarbeiten.
Nicht gleich so freundlich. Ich weiße dich lediglich darauf hin, dass der Post so nicht den @steemstem Regeln entspricht. Sonst in Zukunft bitte den #de-stem Tag weg lassen.
OK, also nichts wirklich eigenes. D.h. kopiert, Wörter weggelassen und etwas anders angeordnet.
Wann hat ihr jemand etwas über den Post Payout gesagt.
Bereich = Anteil an kopierten Inhalten.
Spricht da jetzt die Eifersucht? Muss ich mich jetzt bei dir rechtfertigen von wem ich welche Votes bekomme?
Nicht nur für mich.
Dann halt nicht. Deine Entscheidung.
Dann haben wir bei "schon in einem Bereich" jeweils etwas anderes gemeint.
Wie auch immer. OK, kein Problem, den #de-stem tag in Zukunft wegzulassen.
Ich gebe zu bedenken, dass je selektiver Ihr in Eurem elitären Stem-Zirkel seid, desto isolierter. Die DApp https://www.steemstem.io ist ja schon toter als ein Zombie.
I'm a bit late to the party but I feel it's quite simple. You refer to it as 'selective' and 'elite' - but all it is, is a set of rules the rest of the world has to adhere to for legitimacy. We haven't changed that, we just abide by the same rules.
Whether you're a homeless bum or a wealthy doctor, everyone can enjoy the benefits of what we do... providing they follow the guidelines. There's nothing elite about it.
It only takes maybe 20 minutes to read through the guidelines and make sure your stuff fits.
And regarding steemstem.io being dead, I'm not sure how that's possible, since it simply hosts content from the blockchain, which is still very much alive. The site is not even built to completion so don't expect anything from it for a while yet =)
Naja, stand eigentlich von Anfang an da, egal.
Du kannst den #de-stem Tag in Zukunft gerne benutzen, aber dann halt mit Beiträgen, die nicht von überall her zusammenkopiert sind und unter Einhaltung von Copyright.
Klasse statt Masse. Ansonsten, siehe oben.
Gestern hat sie dir aber noch so gut gefallen, dass du den Tag verwendet hast. Naja, aber da ist bei Steem an jeder Ecke tote Hose.
So schön kann das Leben als Steemit Rentner sein ;-)
Ein !BEER und 6 Trendotoken für Dich !trdo vom rentenbot
beachte bitte den neuen News-Post:
https://steemit.com/deutsch/@rentenbot/wochenpost-bilanz-power-up-tokendepot-und-news
Congratulations @steemrentetoken, you are successfuly trended the post that shared by @stayoutoftherz!
@stayoutoftherz got 6 TRDO & @steemrentetoken got 4 TRDO!
"Call TRDO, Your Comment Worth Something!"
To view or trade TRDO go to steem-engine.com
Join TRDO Discord Channel or Join TRDO Web Site
To view or trade
BEERgo to steem-engine.Hey @stayoutoftherz, here is your
BEERtoken. Enjoy it!Alter, was geht denn hier für ne kranke Scheiße ab? Die Blockwarte sind unterwegs? Schon lange nix Anständiges mehr vor's Rohr gekriegt, ihr Schwanzlutscher?
@stayoutofherz oder wer auch immer. Wenn das hier losgeht, bin ich mit draußen, diesmal aber forever.